Centre Diagnostic et Recherche sur la Granulomatose Septique Chronique (CDiReC) - UF 2393, Laboratoire BEP, Département DBTP, Pôle Biologie, Institut Biologie et Pathologie, CHU Grenoble
Le CDiReC est un des deux centres français experts pour le diagnostic de la granulomatose septique chronique (CGD), appartenant au réseau des laboratoires du Centre de Référence des Déficits Immunitaires (CEREDIH) du Pr A. Fisher à Necker, Paris (https://www.ceredih.fr/locations/laboratories). Il reçoit des prélèvements en provenance des régions Rhône-Alpes, Auvergne, Franche-Comté, Alsace, Lorraine, Aquitaine, Midi-Pyrénées, Provence-Alpes Côte d’Azur, Languedoc-Roussillon, Midi-Pyrénées ainsi que de nombreux pays d’Europe, mais aussi du Maghreb, de Jordanie et d’Amérique du sud.
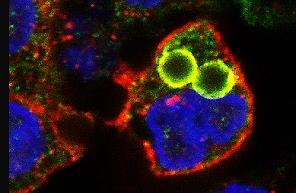 La CGD est une immunodéficience innée rare d’origine génétique, dû à un dysfonctionnement des cellules phagocytaires telles que les monocytes/macrophages, neutrophiles et éosinophiles. C’est une enzymopathie car lors d’infections, la NADPH oxydase des membranes plasmiques de ces cellules est incapable de produire des formes réactives de l’oxygène (FRO) responsables de la microbicidie. Ainsi les bactéries (souvent des gram+ telles que St aureus, Klebsellia, Salmonella) ou les champignons (Aspergillus fumigatus, Candida albicans) seront phagocyter mais non détruits. Il en résulte une accumulation dans les tissus de granulomes (qui ont donné le nom à la maladie) difficiles à réduire par les traitements conventionnels antibiotiques et/ou antifongiques. Les signes cliniques d’immunodéficiences apparaissent très tôt puisque les enfants souffrent d’infections sévères et récidivantes avant l’âge de deux ans généralement (Voir revues Stasia et al., Rev Med Interne 2009 ; 30:221-32, Van den Berg et al. PLoS One 2009;4e5234).
La CGD est une immunodéficience innée rare d’origine génétique, dû à un dysfonctionnement des cellules phagocytaires telles que les monocytes/macrophages, neutrophiles et éosinophiles. C’est une enzymopathie car lors d’infections, la NADPH oxydase des membranes plasmiques de ces cellules est incapable de produire des formes réactives de l’oxygène (FRO) responsables de la microbicidie. Ainsi les bactéries (souvent des gram+ telles que St aureus, Klebsellia, Salmonella) ou les champignons (Aspergillus fumigatus, Candida albicans) seront phagocyter mais non détruits. Il en résulte une accumulation dans les tissus de granulomes (qui ont donné le nom à la maladie) difficiles à réduire par les traitements conventionnels antibiotiques et/ou antifongiques. Les signes cliniques d’immunodéficiences apparaissent très tôt puisque les enfants souffrent d’infections sévères et récidivantes avant l’âge de deux ans généralement (Voir revues Stasia et al., Rev Med Interne 2009 ; 30:221-32, Van den Berg et al. PLoS One 2009;4e5234).
Il est nécessaire de poser le plus tôt possible un diagnostic pour traiter le patient par un traitement anti-infectieux prophylactique qu’il prendra toute sa vie. L’autre alternative est la greffe de moelle allogénique qui nécessite un donneur compatible dans la famille mais elle n’est pas dénuée de risque dans un contexte infectieux et inflammatoire. Des essais de thérapie génique sont actuellement à l’étude en Europe (téléthon 2014). Le Dr Marie José Stasia responsable du CDiReC et le Dr Julie Brault assistante, développent une thérapie protéique pour cette maladie au sein de l’équipe TheREx du laboratoire TIMC/IMAG-UMR CNRS 5525 de l’Université Grenoble Alpes (http://www-timc.imag.fr/rubrique395.html). Grâce à un projet de recherche clinique soutenu par la DRCI du CHU de Grenoble (FibroCGD 2009), la modélisation cellulaire des différentes formes génétiques de la CGD a été obtenue en utilisant les cellules iPSC (induced Pluripotent Stem Cells) provenant des patients pour tester cette nouvelle thérapie (Brault et al. BioResearch Open Access 2014 ; 4:3011-326).
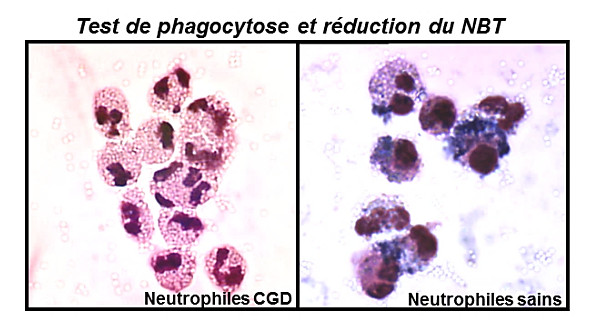 Le diagnostic formel de la maladie est posé grâce aux résultats des tests fonctionnels à partir des neutrophiles du patient, permettant de mettre en évidence le déficit de production des FRO. Les deux principaux tests sont le test de phagocytose et réduction du nitrobleu de tetrazolium (NBT) ou l’analyse par cytométrie de flux du changement de fluorescence de la dihydrorhodamine (DHR). Ils permettent d’évaluer la production des FRO des neutrophiles activés.
Le diagnostic formel de la maladie est posé grâce aux résultats des tests fonctionnels à partir des neutrophiles du patient, permettant de mettre en évidence le déficit de production des FRO. Les deux principaux tests sont le test de phagocytose et réduction du nitrobleu de tetrazolium (NBT) ou l’analyse par cytométrie de flux du changement de fluorescence de la dihydrorhodamine (DHR). Ils permettent d’évaluer la production des FRO des neutrophiles activés.
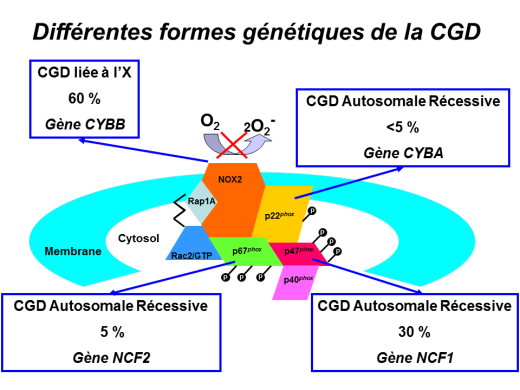 Une fois le diagnostic fonctionnel établi, la recherche de la mutation génique à l’origine de la CGD est entreprise. L’enzyme déficiente NADPH oxydase est un complexe protéique formée de 5 unités principales NOX2 ou gp91phox, p22phox, p47phox et p67phox codées respectivement par les gènes CYBB, CYBA, NCF1 et NCF2. La difficulté est que 4 gènes sont potentiellement impliqués dans la maladie. L’identification du gène muté sera déduite de l’étude d’expression des différentes protéines du complexe NADPH oxydase, par westernblot ou cytométrie de flux. La seconde difficulté est que le type et la localisation de la mutation dans le gène identifié, sont différents pour chaque patient. Ainsi la mise en évidence du défaut génétique impliquent plusieurs approches de biologie moléculaire (Stasia and Li, Semin Immunopathol. 2008 30209-35; Roos et al. Blood Cells Mol Dis. 2010; 44:291-9. Roos et al. Blood Cells Mol Dis. 2010; 45:246-65).
Une fois le diagnostic fonctionnel établi, la recherche de la mutation génique à l’origine de la CGD est entreprise. L’enzyme déficiente NADPH oxydase est un complexe protéique formée de 5 unités principales NOX2 ou gp91phox, p22phox, p47phox et p67phox codées respectivement par les gènes CYBB, CYBA, NCF1 et NCF2. La difficulté est que 4 gènes sont potentiellement impliqués dans la maladie. L’identification du gène muté sera déduite de l’étude d’expression des différentes protéines du complexe NADPH oxydase, par westernblot ou cytométrie de flux. La seconde difficulté est que le type et la localisation de la mutation dans le gène identifié, sont différents pour chaque patient. Ainsi la mise en évidence du défaut génétique impliquent plusieurs approches de biologie moléculaire (Stasia and Li, Semin Immunopathol. 2008 30209-35; Roos et al. Blood Cells Mol Dis. 2010; 44:291-9. Roos et al. Blood Cells Mol Dis. 2010; 45:246-65).
Sites web:
Publications du CDiReC: http://www.ncbi.nlm.nih.gov/pubmed/?term=stasia+m
Contact : Marie José STASIA – PAUGER, PharmD, PhD, HDR,
Centre Diagnostic et Recherche Granulomatose Septique (CDiReC), BEP-DBTP, Pôle Biologie, CHU Grenoble, CS 10217, 38043 Grenoble Cedex 09 - Tél: (+33) (0)4-76-76-54-83 ; Fax: (+33) (0)4-76-76-56-08 ; e-mail: MJStasia@chu-grenoble.fr.